日前,鄭州大學第一附屬醫院肝膽胰外科孫玉嶺教授研究團隊在腫瘤免疫治療方面取得積極進展��。研究團隊發現����,由計算機輔助篩選的佐劑維生素K2���、光敏劑焦脫鎂葉綠酸a(PPA)和DSPE-PEG2000形成的納米顆粒可實現顯著的抗腫瘤活性和免疫微環境重塑�,為癌癥光免疫治療提供了新思路。
研究表明��,利用光動力�、光敏劑在特定激光照射下可以消除癌細胞,并觸發全身免疫反應��,這是腫瘤免疫治療中的一種強大策略���。但是,腫瘤抑制性免疫微環境�����,限制了光敏劑的療效�。為了彌補這種不足,研究團隊首先通過計算模擬和實驗驗證��,確定了維生素K2作為TLR激動劑的配體��,可以有效激活包括樹突狀細胞(DCs)和巨噬細胞在內的抗原呈遞細胞��,并通過TLR途徑促進它們的成熟。然后����,再將維生素K2和焦脫鎂葉綠酸a按照一定比例結合成納米粒。另外�,少許DSPE-PEG2000的加入使納米粒具有更強的親水性和穩定性。精心設計的納米粒不僅具有按需釋放PPA的能力�����,還可以通過釋放維生素K2來激活巨噬細胞向M1型極化和促進DC細胞發育成熟���,進而促進抗原呈遞和CD8+ T細胞的激活�,納米藥物在肝癌�����、乳腺癌等多種癌種中展示了顯著的抗腫瘤效果��。該研究表明�����,計算機輔助的自體佐劑治療策略可作為癌癥光免疫治療一種有效方式。
研究成果以”Molecular simulation-aided self-adjuvanting nanoamplifier for cancer photoimmunotherapy”為題發表在國際權威學術期刊《Theranostics》雜志上���。博士生谷俊謀為論文第一作者��,孫玉嶺教授為責任通訊作者����,遼寧省腫瘤醫院乳腺外科楊世華副教授為共同通訊作者����。
全文鏈接:
https://www.thno.org/v15p2451.htm
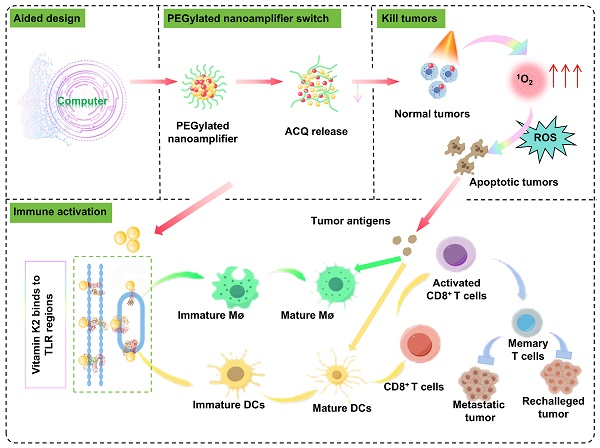
計算機輔助的維生素K2與光敏劑PPA形成的納米顆粒展現出顯著的抗腫瘤活性及免疫微環境重塑能力